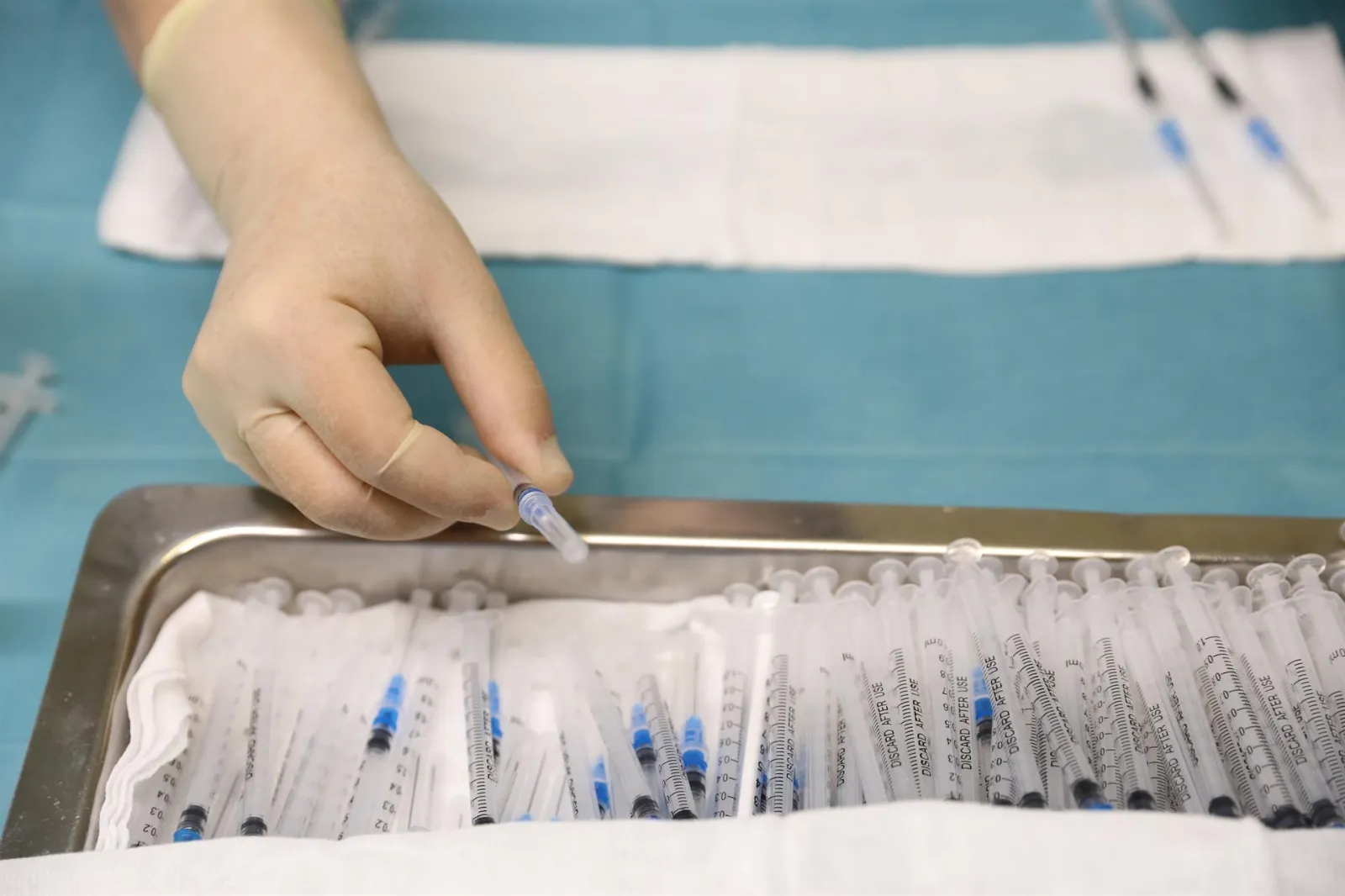
¿En qué se diferencia la vacuna española de las dosis de Pfizer o Moderna?
En la fase definitiva antes de solicitar su comercialización, podría empezar a utilizarse como dosis de refuerzo en próximas campañas de vacunación
La vacuna de Hipra está un paso más cerca de convertirse en la primera vacuna española contra la COVID-19. Ya en fase III del ensayo clínico -autorizado a principios de este mes Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)-, el objetivo es evaluar la seguridad y tolerabilidad de la vacuna de Hipra como dosis de refuerzo, el paso previo necesario para solicitar autorización para su comercialización. Pero ¿en qué se diferencia de las otras dos vacunas que actualmente se administran como dosis de refuerzo?
Pfizer y Moderna son los dos sueros que se están administrando como tercera dosis, algo que podría cambiar con los resultados de esta última fase del ensayo. Si se aprueba la vacuna española. Sanidad podría empezar a utilizarla como dosis extra en próximas campañas de vacunación.
Tal y como explica la Agencia Española de Medicamentos y Productos Sanitarios (Aemps), la vacuna de Hipra frente a la COVID-19 es una vacuna de proteína recombinante adyuvada que contiene la región de unión al receptor de las variantes alfa y beta del SARS-CoV-2, y sería capaz de generar una respuesta inmune frente a diferentes variantes del virus.
Tal y como hemos aprendido durante esta pandemia, las vacunas de Pfizer o Moderna están basadas en la tecnología de ARN mensajero, lo que permite introducir en las células las instrucciones para que generen las proteínas del virus y se produzca la respuesta inmunitaria. Mientras, la vacuna de Hipra es una vacuna de proteínas que se inyectan directamente para generar esa respuesta inmune.
Otra de las ventajas de la vacuna de Hipra es su conservación, ya que en este caso no será necesaria la congelación.